biologiske
introduksjon
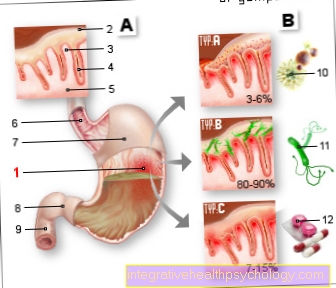
Immunsystemet er essensielt for overlevelse av ethvert menneske. I løpet av evolusjonen har dette utviklet seg til det såkalte adaptive immunsystemet hos mennesker. Dette gir oss muligheten til å reagere mer annerledes og mer effektivt på bakterier og virus. Immunsystemet beskytter oss. Det hjelper oss å overleve kampen med betennelse bedre. Det er mange forskjellige typer betennelsesmodulatorer. For eksempel den såkalte tumor nekrose faktor-alfa, som er forkortet som TNF-α. Sammen med andre faktorer sikrer dette at inflammatoriske celler og tumorceller elimineres før de kan utløse sykdommer.

Men disse "livvakter" i kroppen vår kan også bli "kriminelle". For noen ganger vender immunforsvaret mot oss. I disse tilfellene utvikler det seg autoimmune sykdommer som er vanskelige å behandle med medisiner. Det er her biologikk kommer inn. Biologi kalles også biofarmaceutiske midler eller biofarmasøytiske midler. Dette er medisiner som produseres i genmodifiserte organismer ved bruk av forskjellige metoder for bioteknologi. Eksempler på disse medikamentene er såkalte "monoklonale antistoffer" eller såkalte "fusjonsproteiner". TNF-a-hemmere, blant dem TNF-alfa-reseptorantagonister, tilhører denne gruppen medikamenter.
En kjent biologisk er adalimumab, også kjent under handelsnavnet Humira.
indikasjoner
TNF-a reseptorantagonister brukes ved inflammatoriske, kroniske autoimmune sykdommer. Dette betyr at de er indikert for alle sykdommer der kroppens eget immunforsvar kjemper mot kroppen i stedet for å kjempe for det. I denne prosessen spiller ofte TNF-α en stor rolle. Det sikrer at visse celler begynner å oppføre seg som såkalte fjerningceller (makrofager) og dermed ødelegger vev, bein, brusk og, avhengig av sykdommen, andre kroppsceller.
Spesifikke indikasjoner er for eksempel revmatoid artritt, såkalt juvenil idiopatisk leddgikt, psoriasisartritt, plakkpsoriasis, ankyloserende spondylitt, Crohns sykdom eller ulcerøs kolitt. Biologiske medikamenter, for eksempel TNF-a reseptorantagonister, brukes når ingen andre medikamenter hjelper mot de nevnte sykdommene eller forårsaker for mange bivirkninger.
Biologi for ankyloserende spondylitt
Bechterews sykdom er en inflammatorisk, kronisk autoimmun sykdom. Det tilhører den revmatiske gruppen av former. Det er en av de såkalte spondylartritt. Ved Bechterews sykdom er kroppens eget immunsystem rettet mot bein- og bruskceller i bekken- og ryggområdet og ødelegger dem. Dette kan føre til leddsmerter og deformiteter i de tilsvarende områdene i kroppen. Under visse omstendigheter kan TNF-a reseptorantagonister også brukes. De hemmer messenger-stoffet TNF-α. Siden dette messenger-stoffet spiller en viktig rolle i den inflammatoriske prosessen, blokkeres sykdomsprosessen av TNF-α-hemming. Dette kan lindre symptomene og forsinke progresjonen av sykdommen.
Les mer om emnet på: Terapi av ankyloserende spondylitt
Biologi for psoriasis
Den kollokvise psoriasis er kjent i teknisk sjargong som plakkpsoriasis. Det manifesterer seg som alvorlig flassing av huden med kløe og brennende smerter. Det kan forekomme i forskjellige alvorlighetsgrader. Ved moderat til alvorlig alvorlighetsgrad brukes noen ganger TNF-a reseptorantagonister.
Man snakker om denne alvorlighetsgraden av sykdommen når mer enn 10% av hudoverflaten påvirkes eller hudforandringene dukker opp i spesielt synlige deler av kroppen, for eksempel hender eller ansikt. Et veldig høyt lidelsesnivå fra pasientens side er også et kriterium for klassifisering av moderat til alvorlig psoriasis. I noen tilfeller kan biologikken allerede brukes uten at alle andre aktive ingredienser har sviktet eller tilstedeværelsen av bivirkninger må påvises. TNF-a-reseptorantagonistene kan dempe betennelsesreaksjonene på det punktet hvor de oppstår og dermed forbedre livskvaliteten for den berørte pasienten.
I tillegg kan sekundære sykdommer som kan være et resultat av psoriasis, for eksempel depresjon, forhindres i en viss grad.
Les mer om emnet på: Psoriasis eller psoriasis behandling
Biologi mot ulcerøs kolitt
Ulcerøs kolitt er preget av sterke inflammatoriske, kroniske, periodiske prosesser i tarmslimhinnen og det underliggende bindevevsjiktet. I alvorlige tilfeller dannes magesår. I motsetning til Crohns sykdom påvirkes tykktarmen nesten utelukkende. Også i denne typen autoimmun sykdom kan TNF-a reseptorantagonister påvirke sykdomsforløpet positivt. En rekke forskjellige biologikker er nå godkjent for behandling av ulcerøs kolitt.
Les mer om emnet på: Terapi med ulcerøs kolitt
Biologi for Crohns sykdom
Crohns sykdom er en kronisk inflammatorisk autoimmun sykdom. Kroppens eget forsvarssystem er rettet mot celler i fordøyelseskanalen. Dette kan påvirke hele fordøyelsessystemet fra munnhulen til anus. Her spiller TNF-α en rolle ved at det sikrer at inflammatoriske prosesser og celleødeleggelse skjer. Derfor kan TNF-α-hemmere også dempe sykdomsprosessene i sammenheng med Crohns sykdom og delvis forhindre følgeskader.
Les mer om emnet på: Terapi for Crohns sykdom
Biologi for revmatisme
Mange sykdommer er revmatiske. Når revmatisme brukes på en annen måte, er det vanligvis revmatoid artritt. Dette er en kronisk inflammatorisk autoimmun sykdom der immunceller ødelegger brusk og benceller. Det er leddsmerter og hevelse. Dette skjer ofte i området med fingrene og tærne i metatarsophalangeal ledd. Typisk morgenstivhet forekommer ofte. Også her spiller betennelsesmodulatoren TNF-α en stor rolle. TNF-a reseptorantagonister kan brukes i revmatoidbehandling hvis andre tiltak mislykkes.
Les mer om emnet på: Terapi av revmatoid artritt
Aktiv ingrediens / effekt
De fleste biologikas er proteiner. Det er forskjellige generasjoner av biologikk og derfor også av TNF-a-hemmere. Generasjonene skiller seg fra produksjonen.
Avsluttingen av navnet avslører hvor mye museprotein som fremdeles er til stede i de aktive ingrediensene. Med avslutningen –omab er den 100%, med avslutningen –ximab er det 25% museprotein, med avslutningen - 5-10% er fremdeles tilgjengelig og med avslutningen –umab ingen i det hele tatt. Dette spiller en rolle i toleransen av stoffene.
I tillegg kan TNF-α-hemmerne fungere på forskjellige måter. De kan avskjære TNF-α og dermed forhindre at den binder seg til reseptoren. Som et resultat foregår ikke visse prosesser i cellen som vil føre til den ødeleggende immunreaksjon.En annen mulighet er at TNF-a-hemmeren blokkerer bindingsstedet til TNF-a til reseptoren. Stoffet fungerer da som en såkalt antagonist. Det er også mulig at TNF-α-hemmere fungerer som såkalte fusjonsproteiner. Disse kalles også lokkemottakere. Lokkemottakere er reseptorer som binder ligander, men ikke overfører signaler. TNF-a-lokket reseptorer er oppløselige reseptorer som avskjærer TNF-a før den har nådd sin opprinnelige destinasjon. Som et resultat er det ikke lenger noe signal, og veksten av de ødeleggende immuncellene bremses.
Enbrel®
Den aktive ingrediensen Etanercept er til stede i det kommersielle preparatet Enbrel®. Det er en såkalt lokkemiddelreseptor eller fusjonsprotein. Enbrel® brukes spesielt til revmatisk leddgikt, ungdommelig kronisk leddgikt, psoriasisartritt og såkalt spondylartritt. Psoriasisartritt er en spesiell form for psoriasis som er assosiert med leddsmerter. Enbrel® fungerer som en TNF-a-hemmer ved disse sykdommene, så vel som i noen andre autoimmune sykdommer. Enbrel® er imidlertid ikke effektiv mot Crohns sykdom. Som regel administreres det subkutant en gang i uken med 50 mg eller to ganger i uken med 25 mg.
Les mer om emnet på: Enbrel®
Remicade®
Den aktive ingrediensen infliximab finnes for eksempel i det kommersielle preparatet Remicade®. Infliximab er et kimært monoklonalt antistoff som blokkerer aktiviteten til TNF-α. Siden det er et kimært monoklonalt antistoff, er hovedryggraden menneskelig, og antigenbindingsstedene (25%) er museprotein. Dette betyr at effektiviteten er høyere enn med såkalte murine monoklonale antistoffer, som består av 100% museprotein, og lavere sammenlignet med humaniserte (5-10% museprotein) eller humane monoklonale antistoffer (0% musprotein). Følgelig er risikoen for allergier og intoleranse lavere enn med murine monoklonale antistoffer og høyere enn med humaniserte eller humane antistoffer. Remicade® brukes mot revmatoid artritt, psoriasisartritt, ankyloserende spondylitt og andre autoimmune sykdommer. I motsetning til etanercept er den aktive ingrediensen infliximab også effektiv mot Crohns sykdom. Doseringen er 3-5 mg per kg kroppsvekt, avhengig av sykdommen.
dosering
Siden bilogikas vanligvis er proteiner, må de gis parenteralt (via en infusjon). Oral inntak er ikke mulig fordi kroppen da ville fordøye den og de aktive ingrediensene ikke kunne utvikle effekten. Doseringen avhenger av den aktive ingrediensen og sykdommen som er til stede. Dosen er vanligvis i et til tosifret milligram område og administreres 1-2 ganger i uken.
pris
Kostnadene for biologika er veldig høye. Derfor blir de stort sett bare brukt som en siste utvei. Det vil si hvis alle andre aktive ingredienser som er indikert for de respektive sykdommene, ikke lykkes. Som regel koster to sprøyter rundt 1.600 euro i måneden.
Bivirkninger
Under spesialistbehandling og observasjon er TNF-a-blokkere relativt godt tolererte og trygge medisiner. Som med alle medikamenter kan bivirkninger imidlertid oppstå. Bivirkningene kan deles inn i de som er relatert til applikasjonen og de som er relatert til forstyrrelse av immunforsvaret. Siden biologikken må gis parenteralt (som en infusjon), kan teoretiske reaksjoner oppstå. Sammenlignet med andre biologiske stoffer, skjer dette oftere med virkestoffet infliximab. Men med spesialistbehandling kan disse typer bivirkninger vanligvis kontrolleres godt. Hvis Biologikas gis subkutant (under huden), kan lokale hudreaksjoner utløses. Imidlertid har seponeringen av behandlingen hittil vært svært sjelden nødvendig.
Bivirkninger som oppstår som et resultat av interferens med immunforsvaret er basert på den ytterligere undertrykkelsen av fysiologiske prosesser i kroppen vår. Messenger-stoffet TNF-α er faktisk en viktig betennelsesmodulator. Selv om det delvis er rettet mot immunforsvaret, har det viktige oppgaver knyttet til immunforsvaret. Hvis disse viktige funksjonene til TNF-α blokkeres permanent av medikamenter, kan dette føre til tilsvarende bivirkninger. Følsomheten for infeksjoner kan øke og risikoen for kreft kan også øke ved langvarig bruk. Skader på leveren, nyrene og hjertet kan oppstå. I tillegg kan TNF-α-hemmere reaktivere inaktiv tuberkulose og herpes zoster.
Avhengig av hvilken generasjon av monoklonale antistoffer det er, er risikoen for intoleranse og allergier høyere eller lavere. Dette betyr at jo mer museprotein som fremdeles er til stede i den aktive ingrediensen, jo større er risikoen for allergier og intoleranse. I tillegg kan visse autoantistoffer forekomme. Behandling med en TNF-α-hemmende resulterte sjelden i det som kalles lupus erythematosus. Dette reduserte også igjen når den biologiske behandlingen ble avbrutt. I tillegg er forskjellige sykdommer og tilbakefall i forbindelse med multippel sklerose, samt forverring i tilfelle av uttalt hjerteinsuffisiens, blitt beskrevet.
interaksjon
Hvis det gis vaksinasjoner med levende vaksiner og samtidig TNF-α-hemmere, kan dette utløse sykdom med vaksinepatogenet i stedet for en vaksinasjonseffekt. Videre kan en interaksjon observeres når man kombinerer to biologiske medisiner. For eksempel har dette blitt observert ved samtidig administrering av etanercept og anakinra i løpet av behandlingen for revmatoid artritt. Effekten ble ikke forbedret, men bivirkningene ble potensert. Alvorlige infeksjoner og mangel på visse blodceller utviklet seg, så det som kalles nøytropeni utviklet seg.
Når bør biologi ikke tas?
Hvis det er en tidligere tuberkulosesykdom, skal ingen TNF-α-hemmere brukes. Dette er uavhengig av hvor lenge du hadde tuberkulose. Dette skyldes det faktum at inaktiverte tuberkulosebakterier fremdeles er til stede i kroppen etter at noen har lidd av tuberkulose. Disse tuberkulosebakteriene er inaktive fordi såkalte makrofager overvåker dem. De passer på at bakteriene ikke blir aktive igjen. For at makrofagene skal kunne utføre denne oppgaven, trenger de TNF-α. Hvis dette ikke lenger er tilstrekkelig tilgjengelig for makrofagene på grunn av virkningen av stoffet, kan de ikke lenger utføre oppgaven sin. Som et resultat kan tuberkulosebakteriene bli aktive igjen og reaktivere tuberkulose.
I tillegg er tilstedeværelsen av hepatitt B en kontraindikasjon for behandling med et biologisk middel. Det har vist seg at i dette tilfellet kan behandling med en TNF-a-hemmende reaktivere herpes zoster. Dette manifesterte seg i en økt forekomst av helvetesild og vannkopper hos voksne.
Imidlertid ble det funnet forskjeller i de forskjellige aktive ingrediensene til TNF-a-hemmere. Sykdommene forekom hyppigere hos pasienter behandlet med infliximab, mens disse bivirkningene knapt kunne observeres i terapi med etanercept. Risikoen for reaktivering korrelerte med alderen hos begge sykdommer, med såkalt komorbiditet (tilleggssykdommer) og med tilleggsbehandling med glukokortikoider, for eksempel kortison.
For å beskytte pasienten er det imidlertid foreløpig slik at behandling med en TNF-a-hemmere generelt ikke er tillatt i tilfelle av tidligere tuberkulose eller hepatitt B.
Biologi og alkohol - er de kompatible?
Når du behandler med biologiske stoffer, trenger du ikke gjøre uten alkohol helt. Imidlertid er det erfaringsrapporter der intoleranser er beskrevet. Siden biologikk påvirker funksjonene i nyrene og leveren, er det ganske mulig at alkoholforbruk kan føre til akutt intoleranse. I tillegg kan langvarig alkoholforbruk i kombinasjon med biologiske medisiner øke risikoen for lever- og nyresykdom.
Behandlingskostnad
Kostnadene er veldig høye på grunn av produksjonsprosessen og parenteral administrasjon. TNF-α-hemmere koster rundt 40.000 til 50.000 euro per år. En enkelt applikasjon er minst i det øvre tosifrede området. I tillegg er det personalkostnader, kostnader for forundersøkelser osv. Hvis en spesialist i en praksis eller på en klinikk skulle bestemme at behandling med biolog er den beste behandlingsformen, må han gi en god grunn for dette. Han kan sende inn en søknad til helseforsikringsselskapet for å dekke kostnadene. Behandlingen av søknaden tar vanligvis noen uker. Når søknaden er kontrollert, behandlet og godkjent, betaler helseforsikringsselskapet kostnadene. Det kan imidlertid begrense varigheten av overtakelsen. Et kostnadsforpliktelse blir ofte inngått i første omgang i 3 måneder. Da må en ny søknad sendes.
I 2016 ble de første såkalte biosimilærene for behandling av revmatiske sykdommer offisielt godkjent. Som navnet antyder, ligner de på Biologikas, men ikke de samme som originalen. Noen forfattere antyder at de er et billigere alternativ til biologien. Det er kontroversielt om effekten av dem faktisk tilsvarer originalen. Helseforsikringene håper å spare milliarder i kostnader. Andre eksperter er skeptiske til estimatene. Så langt har biosimilærene bare blitt brukt hos rundt 1-2% av revmatismepasienter. Biosimilærene anbefales av det tyske Society for Rheumatology. Hun fraråder imidlertid å bytte fra originalen til erstatningsproduktet. Siden det ikke foreligger langtidsstudier på dette ennå, kan ikke spesialistsamfunnet ennå ønske en endring i aktive ingredienser på denne måten. Hun fraråder også å ta slike beslutninger bare av hensyn til kostnadene. I tillegg er hun for optimistisk med tanke på vurderingen av kostnadsbesparelsene. Oppsummert kan det sies at det ennå ikke er mulig å estimere hvordan bruken av biologikk vil se ut i fremtiden, til tross for kostnadene.