Enzymer
definisjon

Enzymer er kjemiske stoffer som finnes over hele kroppen. De setter kjemiske reaksjoner i sving i kroppen.
historie
Ordet enzym ble laget av Wilhelm Friedrich Kühne 1878 og er avledet av det greske sminkeordet enzymon, som betyr gjær eller surdeig. Dette fant deretter veien inn i internasjonal vitenskap. De internasjonal union av ren anvendt kjemi (IUPAC) og internasjonal union av biokjemi (IUBMB) jobbet sammen for å utvikle en nomenklatur for enzymer som definerer representantene for denne store gruppen av stoffer som en felles gruppe. Navngivningen, som klassifiserer enzymene i henhold til oppgavene, er viktig for å bestemme oppgavene til de enkelte enzymene.
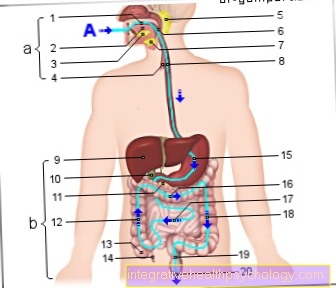
Illustrasjon av enzymer

Enzymer
6 enzymklasser:
- Oxidoreductases
(Oksidasjon / reduksjon) - Overføringer
(Overføring) - Hydrolaser
(Bruk av vann) - Lyases
(Spalting) - Isomeraser
(samme empiriske formel) - Ligaser
(Tilleggsreaksjoner) - Underlag
- Aktivt senter
- Enzym / underlag
komplisert - Enzym / produkt
komplisert
En oversikt over allebilder av Dr-Gumpert finner du på: medisinske illustrasjoner
Navngivning
De Navngivning enzymet er på tre grunnleggende prinsipper basert. Enzymnavn som ender på –ase beskriver flere enzymer i et system. Enzymnavnet beskriver selve reaksjonen som enzymet setter i bevegelse (katalysert). Enzymnavnet er også en klassifisering av enzymet. I tillegg et kodesystem som EF-nummersystem, der enzymene er laget under en numerisk kode fire tall kan bli funnet. Det første tallet indikerer enzymklassen. Lister over alle oppdagede enzymer sikrer at den angitte enzymkoden kan bli funnet raskere. Selv om kodene er basert på egenskapene til reaksjonen som enzymet katalyserer, viser det seg i praksis at tallkoder er uhåndterlige. Systematiske navn basert på reglene ovenfor brukes oftere. Problemer med nomenklaturen oppstår for eksempel med enzymer som katalyserer flere reaksjoner. Derfor er det noen ganger flere navn på dem. Noen enzymer har trivielle navn som ikke indikerer at stoffet som er nevnt er et enzym. Siden navnene tradisjonelt har blitt mye brukt, har noen av dem blitt beholdt.
Klassifisering etter enzymfunksjon
I henhold til IUPAC og IUBMB er enzymer delt inn i seks enzymklasser i henhold til reaksjonen de satte i gang:
- Oxidoreductases
Oxidoreductases setter i gang redoksreaksjoner. I denne kjemiske reaksjonen overføres elektroner fra den ene reaksjonspartneren til den andre. Ett stoff frigjør elektroner (oksidasjon) og et annet stoff aksepterer elektroner (reduksjon).
Formelen for den katalyserte reaksjonen er A ?? + B? A? + B?.
Stoff A frigjør et elektron (?) Og oksideres, mens stoff B absorberer dette elektronet og reduseres. Dette er grunnen til at redoksreaksjoner også kalles reduksjons-oksidasjonsreaksjoner.
Mange metabolske reaksjoner er redoksreaksjoner. Oksygenaser overfører ett eller flere oksygenatomer til underlaget. - Overføringer
Transferaser overfører den funksjonelle gruppen fra ett substrat til et annet. Funksjonelle grupper er atomgrupper i organiske forbindelser som i stor grad bestemmer stoffets egenskaper og reaksjonsatferd. Kjemiske forbindelser som har samme funksjonelle grupper er gruppert i stoffklasser på grunn av deres lignende egenskaper. Funksjonelle grupper vil bli delt inn i henhold til om de er heteroatomer eller ikke. Heteroatomer er alle atomer i organiske forbindelser som verken er karbon eller hydrogen.
F.eks .: -OH -> hydroksylgruppe (alkoholer) - Hydrolaser
Hydrolaser deler bindingene i reversible reaksjoner ved bruk av vann. Estere, estere, peptider, glykosider, syreanhydrider eller C-C bindinger. Likevektsreaksjonen er: A-B + H2O? A-H + B-OH.
Et enzym som tilhører gruppen hydrolaser er for eksempel alfa-galaktosidase. - Lyases
Lyaser, også kalt syntaser, katalyserer spaltingen av komplekse produkter fra enkle underlag uten å splitte av ATP. Reaksjonsskjemaet er A-B → A + B.
ATP er adenosintrifosfat og et nukleotid, bestående av trifosfat av nukleosidet adenosin (og som sådan en energirik byggestein av nukleinsyren RNA). Imidlertid er ATP hovedsakelig den universelle formen for umiddelbart tilgjengelig energi i hver celle og samtidig en viktig regulator for energiforsyningsprosesser. Om nødvendig blir ATP syntetisert fra andre energilagre (kreatinfosfat, glykogen, fettsyrer). ATP-molekylet består av en adeninrest, sukkerribosen og tre fosfater (? To?) I ester (?) Eller anhydridbindinger (? Og?). - Isomeraser
Isomeraser akselererer den kjemiske omdannelsen av isomerer. Isomerisme er forekomsten av to eller flere kjemiske forbindelser med nøyaktig de samme atomer (samme empiriske formel) og molekylvekter, som imidlertid er forskjellige i forbindelsen eller den romlige oppstillingen av atomene. De tilsvarende forbindelsene kalles isomerer.
Disse isomerer er forskjellige i kjemiske og / eller fysiske, og ofte også i biokjemiske egenskaper. Isomerisme forekommer primært med organiske forbindelser, men også med (uorganiske) koordineringsforbindelser. Isomerismen er delt inn i forskjellige områder. - Ligaser
Ligaser katalyserer dannelsen av stoffer som er kjemisk mer komplekse enn substratene som brukes, men i motsetning til lyasene er de bare enzymatisk effektive ved ATP-spaltning. Dannelsen av disse stoffene krever derfor energi, som oppnås ved splitting av ATP.
Noen enzymer er i stand til å katalysere flere, noen ganger veldig forskjellige, reaksjoner. Hvis dette er tilfelle, blir de tildelt flere enzymklasser.
Du kan også være interessert i disse artiklene:
- Alfa-glukosidase
- Lipase
- Trypsin
Klassifisering i henhold til enzymstruktur
Nesten alle enzymer er proteiner og kan klassifiseres basert på lengden på proteinkjeden:
- Monomerer
Enzymer som bare består av en proteinkjede - Oligomerer
Enzymer som består av flere proteinkjeder (monomerer) - Multi-enzymkjeder
Flere aggregerte enzymer som samarbeider og regulerer hverandre. Disse enzymkjedene katalyserer de påfølgende trinnene i cellens metabolisme.
I tillegg er det individuelle proteinkjeder som inneholder flere enzymaktiviteter; disse blir referert til som multifunksjonelle enzymer.
Klassifisering etter medfaktorer
En annen klassifisering er klassifiseringen etter hensynet til kofaktorene. Kofaktorer, koenzymer og ko-substrater er navn på forskjellige klassifiseringer av stoffer som påvirker biokjemiske reaksjoner gjennom deres interaksjon med enzymer.
Organiske molekyler og ioner (for det meste metallioner) blir vurdert.
De rene proteinenzymer består utelukkende av proteiner, og det aktive senteret er bare dannet av aminosyrerester og peptidrygraden. Aminosyrer er en klasse av organiske forbindelser med minst en karboksygruppe (-COOH) og en aminogruppe (-NH2).
Holoenzymer består av en proteinkomponent, apoenzymet, og en kofaktor, et molekyl med lav molekylvekt (ikke et protein). Begge deler er viktige for enzymets funksjon.
Koenzymer
Organiske molekyler som medfaktorer kalles koenzymer. Hvis de er kovalent bundet til apoenzymet, kalles de protesegrupper eller co-substrater. En protesegruppe refererer til ikke-proteinkomponenter som er fast (hovedsakelig kovalent) bundet til et protein med en katalytisk effekt.
Kosubstrater er navn på forskjellige klassifiseringer av stoffer som påvirker biokjemiske reaksjoner gjennom deres interaksjon med enzymer. Som biokatalysatorer akselererer molekyler reaksjoner i organismer, enzymer akselererer biokjemiske reaksjoner. De reduserer aktiveringsenergien som må overvinnes slik at stoffet kan omdannes.